「硫酸」:各本之異
| [底本] | [底本] |
刪去的內容 新增的內容
細 Robot: Adding jv:Asam sulfat |
細 Bot: Migrating 70 interwiki links, now provided by Wikidata on d:q4118 (translate me) |
||
| 第三六行: | 第三六行: | ||
[[Category:化學]] |
[[Category:化學]] |
||
{{stub}} |
{{stub}} |
||
[[ar:حمض الكبريتيك]] |
|||
[[az:Sulfat turşusu]] |
|||
[[be:Серная кіслата]] |
|||
[[bg:Сярна киселина]] |
|||
[[bn:সালফিউরিক এসিড]] |
|||
[[br:Trenkenn sulfurek]] |
|||
[[bs:Sumporna kiselina]] |
|||
[[ca:Àcid sulfúric]] |
|||
[[cs:Kyselina sírová]] |
|||
[[cy:Asid swlffwrig]] |
|||
[[da:Svovlsyre]] |
|||
[[de:Schwefelsäure]] |
|||
[[el:Θειικό οξύ]] |
|||
[[en:Sulfuric acid]] |
|||
[[eo:Sulfata acido]] |
|||
[[es:Ácido sulfúrico]] |
|||
[[et:Väävelhape]] |
|||
[[eu:Azido sulfuriko]] |
|||
[[fa:سولفوریک اسید]] |
|||
[[fi:Rikkihappo]] |
|||
[[fr:Acide sulfurique]] |
|||
[[ga:Aigéad sulfarach]] |
|||
[[gl:Ácido sulfúrico]] |
|||
[[he:חומצה גופרתית]] |
|||
[[hi:गन्धकाम्ल]] |
|||
[[hr:Sumporna kiselina]] |
|||
[[hu:Kénsav]] |
|||
[[id:Asam sulfat]] |
|||
[[is:Brennisteinssýra]] |
|||
[[it:Acido solforico]] |
|||
[[ja:硫酸]] |
|||
[[jv:Asam sulfat]] |
|||
[[ka:გოგირდმჟავა]] |
|||
[[kk:Күкірт қышқылы]] |
|||
[[ko:황산]] |
|||
[[la:Acidum sulphuricum]] |
|||
[[lmo:Acid sulforich]] |
|||
[[lt:Sieros rūgštis]] |
|||
[[lv:Sērskābe]] |
|||
[[ml:സൾഫ്യൂരിക് അമ്ലം]] |
|||
[[ms:Asid sulfurik]] |
|||
[[my:ဆာလဖျူရစ်အက်ဆစ်]] |
|||
[[nds:Swevelsüür]] |
|||
[[nl:Zwavelzuur]] |
|||
[[nn:Svovelsyre]] |
|||
[[no:Svovelsyre]] |
|||
[[oc:Acid sulfuric]] |
|||
[[pl:Kwas siarkowy]] |
|||
[[pnb:گندھک دا تیزاب]] |
|||
[[pt:Ácido sulfúrico]] |
|||
[[ro:Acid sulfuric]] |
|||
[[ru:Серная кислота]] |
|||
[[sh:Sumporna kiselina]] |
|||
[[si:සල්ෆියුරික් අම්ලය]] |
|||
[[simple:Sulfuric acid]] |
|||
[[sk:Kyselina sírová]] |
|||
[[sl:Žveplova kislina]] |
|||
[[sq:Acidi sulfurik]] |
|||
[[sr:Сумпорна киселина]] |
|||
[[sv:Svavelsyra]] |
|||
[[ta:கந்தகக் காடி]] |
|||
[[th:กรดซัลฟิวริก]] |
|||
[[tr:Sülfürik asit]] |
|||
[[uk:Сульфатна кислота]] |
|||
[[ur:ترشۂ گندھک]] |
|||
[[vec:Àsido solfòrico]] |
|||
[[vi:Axít sunfuric]] |
|||
[[zh:硫酸]] |
|||
[[zh-min-nan:Liû-sng]] |
|||
[[zh-yue:硫酸]] |
|||
二〇一三年三月一四日 (四) 〇八時三三分審
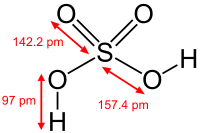
硫酸,(化學式H2SO4),硫酸性烈,偏分子化合物也,屬酸。三酸兩鹼處一焉。
別名漒水、鏹水、綠矾油。
故所謂綠矾油也,蓋餾綠矾(硫酸亞鐵,硫酸成鹽之一也。)出油,故名之。

有用實蕃,古人譽曰「化學工業之母」也。
性
- 狀:純硫酸稠而似油也。
- 味:一說無味,一說少甘。
- 密度:一點八四公克每毫升。
- 熔沸點:熔點十點四攝氏度也。沸點,純者二百九十攝氏度也,零點九八者[一]三百三十八攝氏度也。
- 溶解:與水互溶焉。
- 電解質:然。
- 酸性:然。
- 吸水性:(濃)遇水生溫,放熱。
- 脫水性:(濃)遇物之有氫氧者,則奪之以為水也。
- 氧化性:(濃)然。
製備
意外處理
其之濺身,當以乾布拭去,并輔以小蘇打。勿以水,其遇水生熱而將灼傷也。
有用
反應
複分解反應:如:2NaOH+H2SO4===Na2SO4+2H2O以彰酸之通性
